值得收藏!如何办理第二类医疗器械经营备案?
更新:2025-01-16 07:00 编号:28831698 发布IP:117.61.15.33 浏览:21次









- 发布企业
- 陕西锦强企业管理有限公司商铺
- 认证
- 资质核验:已通过营业执照认证入驻顺企:第2年主体名称:陕西锦强企业管理有限公司组织机构代码:91610125MAD53XMYXM
- 报价
- 请来电询价
- 办理时间
- 3-5天
- 服务优势
- 流程短、出证快
- 价格优势
- 诚信真实
- 关键词
- 医疗器械经营许可证,第二类医疗器械,如何办理第二类医疗器械,医疗器械经营备案,医疗器械备案资料
- 所在地
- 陕西省西安市鄠邑区甘亭街道崇立·嶺秀城6号楼2单元20202室
- 手机
- 17792408819
- 联系人
- 田梦 请说明来自顺企网,优惠更多
详细介绍
本文以苏州为例对第二类医疗器械经营备案的办理要求、办理流程、材料清单和网上申报进行说明。
一、办理要求
办理第二类医疗器械经营备案之前,很多人可能会问需要租赁多大的场地?要雇多少人?人员资质有什么要求?针对这些问题,苏州市食品药品监督管理局2017年1月发布了《关于实施医疗器械经营质量管理规范的通知》,对上述问题进行了较明确的解答。下附全文:
为深入贯彻实施《医疗器械经营质量管理规范》,根据《医疗器械监督管理条例》、《医疗器械经营监督管理办法》、《医疗器械经营质量管理规范》及《医疗器械经营质量管理规范现场检查指导原则》等有关规定,结合苏州实际,对《医疗器械经营质量管理规范》部分条款要求作明确,制定本意见。
一、市场主体资格
医疗器械经营企业申请许可或备案时,应当符合《医疗器械经营质量管理规范》要求。申办主体应当是企业组织,包括法人企业、非法人企业、个人独资、合伙制企业等。企业分公司、分支机构的申办要求同普通申办主体。融资租赁类公司如需从事医疗器械批发、零售等业务活动的应申请许可或备案,申办要求同普通申办主体,仅从事医疗器械融资租赁类业务无需申请许可或备案。医疗器械经营企业申请许可或备案时应先取得《营业执照》,并有相应的经营范围。
二、人员与培训
(一)关于企业负责人、质量管理人员等在职在岗要求
企业负责人及从事质量管理工作的人员应当在职在岗,有效履行相应职责。质量管理机构人员及不设质量机构的企业中的质量负责人应为企业内专职质量管理人员,不能由企业负责人及经营部门负责人兼任,可在本企业内兼任验收、技术服务、行政管理等不影响其履行质量管理职责的工作。质量管理机构负责人可由质量负责人兼任。兼营医疗器械的零售药店的药品质量负责人符合要求的可兼任医疗器械质量负责人。
(二)关于质量管理人员配备数量
从事第三类医疗器械批发业务的企业、医疗器械零售连锁企业(总部)、医疗器械委托贮运企业,应当设置质量管理机构。质量管理机构至少由1名质量管理机构负责人和1名质量管理人员组成,医疗器械委托贮运企业除质量管理机构负责人外,至少配备2名质量管理人员。除上述类别的医疗器械经营企业应当至少配备1名企业质量负责人。
(三)关于质量管理人员学历或资质要求
从事第二类、第三类医疗器械批发业务和第三类医疗器械零售业务的企业,其质量负责人、质量管理机构负责人应当具备医疗器械相关(相关指医疗器械、生物医学工程、机械、电子、医学、生物工程、化学、药学、护理学、康复、检验学、计算机、法律、管理等,下同)大专以上学历或者中级以上技术职称,应当具有3年以上医疗器械经营质量管理工作经历。
专营第二类医疗器械的零售企业,其质量负责人应当具有医疗器械相关中专以上学历或初级以上技术职称。兼营第二类医疗器械的零售企业,应当配备1名高中以上学历,经医疗器械法规及所经营的医疗器械技术培训的质量管理人员。
从事体外诊断试剂的质量管理人员(含质量负责人)中,应当有1人为主管检验师,或具有检验学相关(相关指医学检验、基础医学、临床医学、医学技术、生物医学工程、生物工程、生物科学、化学、药学等,下同)大学以上学历并从事检验相关工作3年以上工作经历。从事体外诊断试剂验收和售后服务工作的人员,应当具有检验学相关中专以上学历或者具有检验师初级以上技术职称。
(四)关于经营人员学历或资质要求
从事植入和介入类医疗器械经营人员中,应当配备至少1名医学相关(相关指基础医学、预防医学、临床医学、医学技术、口腔医学、中医学、护理学等)大专以上学历,并经过生产企业或者供应商培训的人员。从事角膜接触镜验配企业的经营人员中,应当配备至少1名具有相关(相关指基础医学、临床医学、医学技术、护理学、医疗器械、光学、视光学、眼视光技术等)或者具有验光员资质的人员。从事助听器验配企业的经营人员中,应当配备至少1名具有相关(相关指基础医学、临床医学、医学技术、护理学、医疗器械、听力学等)或者经产品相关生产企业培训合格的验配师资质人员。
主营范围为家用高频仪器设备、物理治疗及康复设备等的零售企业,应配备每门店至少1名专职医师或护师以上技术人员。
上述人员可由企业负责人、质量负责人或公司其它岗位人员兼任。
(五)关于企业人员体检的要求
企业应当建立员工健康档案,质量管理、验收、库房管理等直接接触医疗器械岗位的人员,应当至少每年进行一次健康检查。健康体检应在苏州大市范围的机构进行,并出具经盖章确认的、有效的体检报告书。
三、设施与设备
(一)关于经营场所
企业应当具有与经营范围和经营规模相适应、独立的经营场所,经营场所的面积应当满足经营要求。经营企业“经营场所”应当与营业执照中的“住所”一致。鼓励经营企业入驻产业园、科技园、企业孵化器、创客空间等新兴产业聚集区,对营业执照中的“住所”在产业园、科技园、企业孵化器、创客空间等地的经营企业允许“住所”之外另设一处经营场所,企业经营场所应设置在住所所在的市辖区(市)行政管辖区内。
医疗器械批发企业、医疗器械零售连锁企业(总部)经营场所面积不得少于50平方米(不含仓库,以实际使用面积计算,下同)。医疗器械零售门店(含医疗器械零售连锁门店)其经营场所面积不得少于20平方米,兼营医疗器械,应设有医疗器械专区或专柜。经营场所应设在门面房或其它方便消费者购买商业用房内。
主营范围为家用高频仪器设备、物理治疗及康复设备等的零售企业,经营场所面积不得少于100平方米。
经营需验配等特殊要求医疗器械产品的企业,应当设置满足其特殊要求的区域,配备相适应的设施、设备。如经营软性角膜接触镜的企业,在其经营场所应当设有检查区、验配区等,配备电脑验光仪、裂隙灯显微镜等仪器设备;如经营助听器的企业,在其经营场所应当设有听力测试室、验配区等,配备听力测试仪器等与其经营相适应的专用设备。
(二)关于库房
企业应当具有与经营范围和经营规模相适应、独立的库房,库房的面积应当满足经营要求。库房的条件、设施设备应当按照说明书或标签标示的要求,符合贮存的医疗器械产品特性。
医疗器械批发企业、医疗器械零售连锁经营企业(总部),若库房地址与经营场所同址或邻址的(同一或相邻门牌号,下同),库房面积不得少于20平方米;若库房地址与经营场所异址的,库房面积不少于40平方米。
医疗器械经营企业从事体外诊断试剂批发业务的,应根据自身经营体外诊断试剂品种的贮存条件确定是否需要冷藏或冷冻。经营需要冷藏或冷冻经营体外诊断试剂的企业,若库房地址与经营场所同址或邻址的,库房面积不得少于100平方米;若库房地址与经营场所异址的,库房面积不少于150平方米。仓库应设置容积不小于20立方米的冷库。如经营品种仅需常温贮存或企业对冷藏、冷冻品种委托其他企业贮存的可不设冷库,按一般医疗器械批发企业面积要求设置库房。
按照《医疗器械经营质量管理规范》第十八条规定,可以不单独设立医疗器械库房的企业,不在此列。
从事医疗器械零售业务的经营企业,如无需要,可不设仓库。
对于全部委托其他企业进行存储的企业,可不设仓库。
(三)关于委托贮运
对于全部委托或部分委托其他企业进行存储的企业,在办理《医疗器械经营许可证》时需另行提供相关资料,包括:
1、贮存、配送服务协议;
2、由药监部门出具的受托企业的委托贮存、配送资质;
3、经营场所与库房之间医疗器械进、销、存信息实时传输功能的计算机管理系统(能远程监控产品在库情况,包括医疗器械产品入库、产品库存、产品出库等信息。有条件的企业还应做到库房温湿度在线监测、产品运输状况监测);
4、委托贮存、配送的质量管理制度;
5、食药监部门要求的其他材料。
委托其他企业进行贮存、配送的,《医疗器械经营许可证》、《第二类医疗器械经营备案凭证》的“仓库地址”项下需标注承接贮存的库房地址、承接委托的经营企业名称以及是全部委托还是部分委托。
经营企业拟增加“提供贮存、配送服务”经营模式的,按《苏州市医疗器械产品委托贮存配送经营企业管理要求》(见附件)规定的要求办理。
(四)关于异地设库
经营企业的住所(经营场所)与仓库地址设置在不同省辖市行政管辖区内的,如果企业住所在苏州,仓库不在苏州,则向住所所在地区(市)局(苏州市局对此事项的委托办理部门,下同)提出申请,仓库设置应满足苏州市要求(《医疗器械经营质量管理规范》与本通知要求)以及仓库所在地食药监部门的要求。如果企业住所不在苏州,仓库在苏州的,则按住所所在地食药监部门要求办理,仓库设置应满足苏州市要求。
本意见自2017年2月19日起正式施行。原《苏州市食品药品监督管理局关于医疗器械许可及备案有关事宜通知》(苏食药检监许可[2015]1号)废止。法律、法规、规章及上级文件另有规定的,从其规定。
二、办理流程
在江苏省政务服务网上进行申报,审批通过后递交纸质材料至办理窗口(下附地址和联系方式),领取备案凭证。
| 序号 | 单位 | 地址 | 咨询电话 |
| 1 | 姑苏区行政服务中心 | 姑苏区解放东路117号 | 0512-65852167 |
| 2 | 相城区行政服务中心 | 相城区庆元路168号 | 0512-67592302 |
| 3 | 吴中区行政服务中心 | 吴中区苏街198号(吴中经济开发区) | 0512-65636733 |
| 4 | 吴江区市场监督管理局 | 吴江区中山南路1788号 | 0512-63983212 |
| 5 | 工业园区市场监督管理局 | 园区翠园路151号工商大厦807室 | 0512-66600636 0512-66600871 |
| 6 | 高新区市场监督管理局 | 高新区科普路50号 | 0512-68753052 |
| 7 | 张家港市市场监督管理局 | 张家港市人民中路30号1号楼611 | 0512-58187920 |
| 8 | 昆山市行政服务中心 | 昆山市前进中路219号 | 0512-57379042 |
| 9 | 常熟市市场监督管理局 | 常熟市新世纪大道87号 | 0512-52895231 |
| 10 | 太仓市市场监督管理局 | 太仓市东亭南路55号 | 0512-53522731 |
| 11 | 张家港保税区市场监管局 | 张家港市金港镇长江中路140号 | 0512-58358733 |
三、材料清单及模板
办理所需的材料清单、模板及相关要求参见第二类医疗器械经营备案材料须知(20220516版)。具体内容可点击链接跳转,主要内容摘录如下:
3.1 办理清单
0. 营业执照(仅在申报系统提交电子版,)
1.第二类医疗器械经营备案表;
2.法定代表人、企业负责人、质量负责人、技术人员的身份证明、学历或者职称证明复印件;
3.企业组织机构与部门设置说明;
4.医疗器械经营范围、经营方式;
5.经营场所和库房的地理位置图、平面图、房屋产权文件或者租赁协议复印件;
6.主要经营设施、设备目录;
7.经营质量管理制度、工作程序文件目录、GSP自查表等;
8.经办人授权证明文件。
3.2 具体要求
1.第二类医疗器械经营备案表
1.1按照实际内容填写,不涉及的可缺项,填写“/”。其中,企业名称、注册资本、统一社会信用代码、成立日期、住所、法定代表人等按照营业执照内容填写。
1.2经营场所
“经营场所”应按“市名+区名+路名+门牌号+楼层+室号”顺序登载。
1.3库房地址
“库房地址”应按“市名+区名+路名+门牌号+楼层+室号”顺序登载。
零售门店无仓库的,用“******”代替,不得留白。
1.4经营方式指批发、零售、批零兼营、为医疗器械注册人、备案人和经营企业专门提供运输、贮存服务。
1.5经营范围应当按照国家药品监督管理部门发布的医疗器械分类目录中规定的管理类别、分类编码及名称填写。经营范围不得只填写“Ⅱ类医疗器械”等统称。
若经营产品为分类目录2002版产品,则申请时填在经营范围中填写分类目录2002版编码;若经营产品为新《分类目录》产品,则申请时填在经营范围中填写新《分类目录》编码。
2.法定代表人、企业负责人、质量负责人、技术人员的身份证明、学历或者职称证明复印件
2.1员工名册。
必须提供企业所有人员的情况。
2.2企业法定代表人
材料包括:①身份证。
(注:企业法定代表人身份证明可以是护照)。
2.3企业负责人
材料包括:①身份证;②人员简历表;③在职在岗证明;④体检证明。
2.4质量负责人
资质材料包括:①身份证;②学历证书或职称证明复印件;③人员简历表、④在职在岗证明;⑤体检证明。
质量负责人应当具备医疗器械相关(相关指医疗器械、生物医学工程、机械、电子、医学、生物工程、化学、药学、护理学、康复、检验学、计算机、法律、管理等)。
专营第二类医疗器械的零售企业,其质量负责人应当具有医疗器械相关中专以上学历或初级以上技术职称。兼营第二类医疗器械的零售企业,应当配备1名高中以上学历,经医疗器械法规及所经营的医疗器械技术培训的质量管理人员。
2.5 质量管理人员
质量管理人员均需要填写(兼职的不重复提供),包括质量管理机构负责人、质量管理员、验收养护人员、售后服务人员等涉及经营管理质量的人员。
资质材料包括:①身份证;②学历证书或职称证明复印件;③人员简历表、④在职在岗证明;⑤体检证明。
2.6技术人员的质量管理、经营等关键岗位人员
2.6.1从事体外诊断试剂的质量管理人员中,应当有1人为主管检验师,或具有检验学相关(相关指医学检验、基础医学、临床医学、医学技术、生物医学工程、生物工程、生物化学、化学、药学等,下同)大学以上学历并从事检验相关工作3年以上工作经历。从事体外诊断试剂验收和售后服务工作的人员,应当具有检验学相关中专以上学历或者具有检验师初级以上技术职称。
2.6.2从事植入(6846)和介入类(6877)医疗器械经营人员中,应当配备医学相关(相关指基础医学、预防医学、临床医学、医学技术、口腔医学、中医学、护理学等)大专以上学历,并经过生产企业或者供应商培训的人员。
资质材料包括:①身份证;②学历证书或职称证明复印件;③人员简历表、④在职在岗证明;⑤体检证明;⑥生产(供应)商培训证明。
2.6.3从事角膜接触镜、助听器等其他有特殊要求的医疗器械经营人员中,应当配备具有相关(相关指基础医学、临床医学、医学技术、护理学、医疗器械、听力学等)或者职业资格的人员。
资质材料包括:①身份证;②学历证书或职称证明复印件;③人员简历表、④在职在岗证明;⑤体检证明;⑥零售企业的验配人员(如验光员、医师或护师)的资格证书。
2.6.4其他说明
①学历证书真伪请各单位自行到学信网查询(http://www.chsi.com.cn),依次进入学籍学历查询-零散查询。查询免费。各企业应对提供本材料的真实性负责。
②体检证明一年内有效。
③原则上在职在岗证明一般为shebao证明、劳动合同等。
④企业负责人和质量管理人员需要了解医疗器械基本法律法规,一般在现场提交资料或者现场检查时进行测试。
⑤简历部分学习经历填写终学历,工作部分应如实填写曾经工作的工作单位,时间要连续。
3.企业组织机构与部门设置说明
需要列明组织机构图,以及部门的职责。
4.医疗器械经营范围、经营方式(根据申报界面申请自动生成)
5.经营场所和库房的地理位置图、平面图、房屋产权文件或者租赁协议复印件
5.1地理位置图可以用百度地图的截图,截图中至少包含四个主要道路。
5.2平面图要包含企业名称、地址(到楼层)等信息和实际使用面积(标注长宽)。
5.3房屋产权证明文件为房产证,用途应为“非住宅”。经营场所不得设在居民住宅内、budui营区(不含可租赁区)以及其他不适合经营的场所。
5.4企业不设仓库,委托其他企业运输、贮存的,提供委托储运合同复印件、受托方资质文件。
6.主要经营设施、设备目录
主要包括办公桌、文件柜、电脑、打印机、空调、灭火器、灭鼠笼、温湿度计、地垫、货架、冷库、冷柜、电冰箱、计量仪器等用于经营和库房的设施设备。
7.经营质量管理制度、工作程序、GSP自查表等文件
7.1经营质量管理制度、工作程序文件目录应包括符合GSP要求的所有制度文件以及相应的工作程序文件目录。
委托其他企业运输、贮存的,需特别体现委托相关制度目录。
7.2医疗器械经营质量管理规范企业自查表。
医疗器械GSP检查情况表
说明:请企业对照《医疗器械GSP检查情况表》的条款逐条填写,后将不合格项目填入《医疗器械经营质量管理规范企业自查表》中汇总。
8.信息管理系统基本情况介绍和功能说明
委托其他企业运输、贮存的,需特别说明系统互通情况。
9.经办人授权文件
法定代表人本人办理的可以不提供本材料。
其他说明
.申报前请先领取《营业执照》,《营业执照》中的“经营范围”必须包括:“医疗器械经营”、“医疗器械零售”、“医疗器械批发”、“销售医疗器械”等含义的字样。如没有,请先增加《营业执照》经营范围。
四、网上申报
第二类医疗器械经营备案需要在江苏省政务服务网上进行线上申请,具体的申请路径如下
进入江苏省政务服务网首页,主页搜索第二类医疗器械经营备案(图1),跳转到搜索结果界面(图2);
2.单击第二类医疗器械备案办事指南(图2),选择相应的设区市(图3)进入办事指南界面,办事指南页提供了备案所需的材料清单及模板,单击右上角的在线办理(图4);
3. 进入申报界面前会要求用户先登录,建议选择法人方式登录,如无账号,先行注册账号。(图5)
4.登录成功后,选择营业执照住所所在的区县进入申报界面,该页同样提供了填报记录,从中可以看到各申请当前的状态。点击每条填报记录左侧的查看,可以查看该记录详细申报信息及审核意见(!!!)(图6)
5. 申报
5.1 填写备案申报信息(图7),单击保存,
5.2 填写附属信息,单击保存
5.3点击各项材料右侧的“未上传”上传相应的附件,将所有材料(含营业执照)打包后,通过单击页面顶部的“选择要上传的文件”进行上传。后点击保存,即完成申报。(图8)
6. 系统显示提交成功,通过步骤4,可看到该申请显示为待受理状态
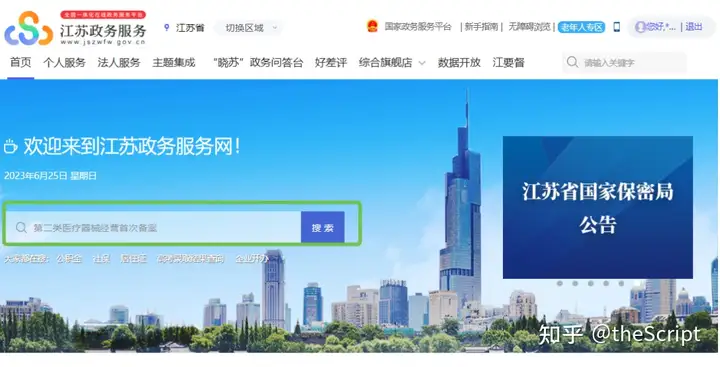
图1 主页搜索第二类医疗器械备案
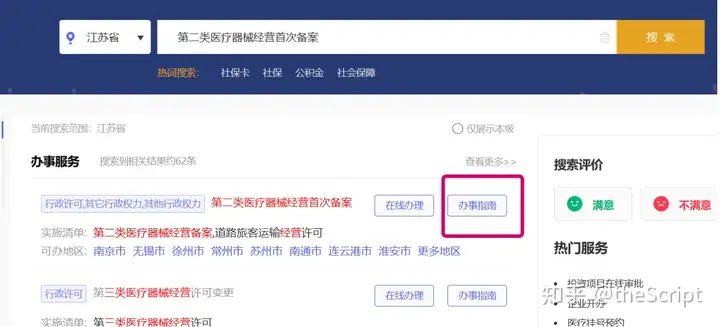
图2 办事指南
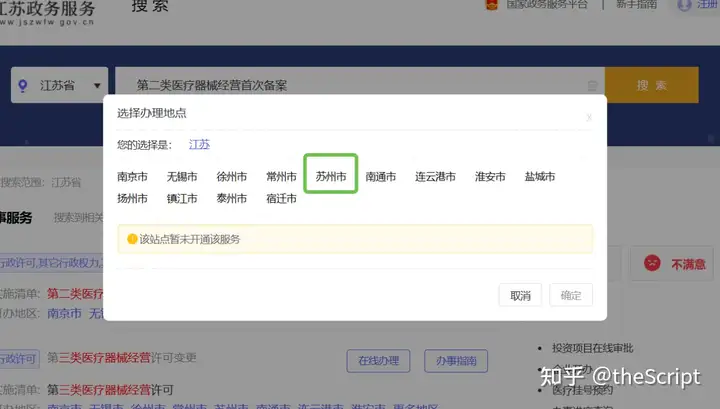
图3 选择设区市

图4 材料清单及在线办理
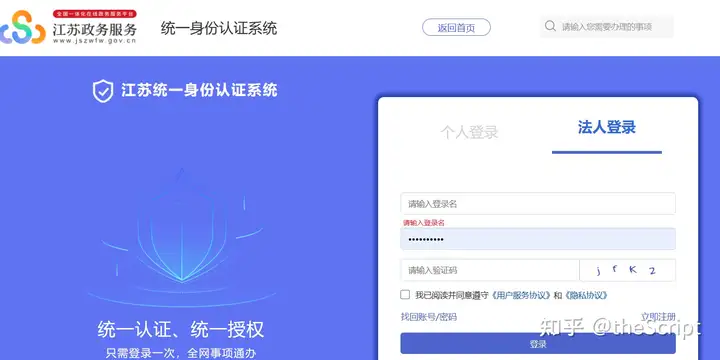
图5 登录账号

图6 区县选择和填报记录
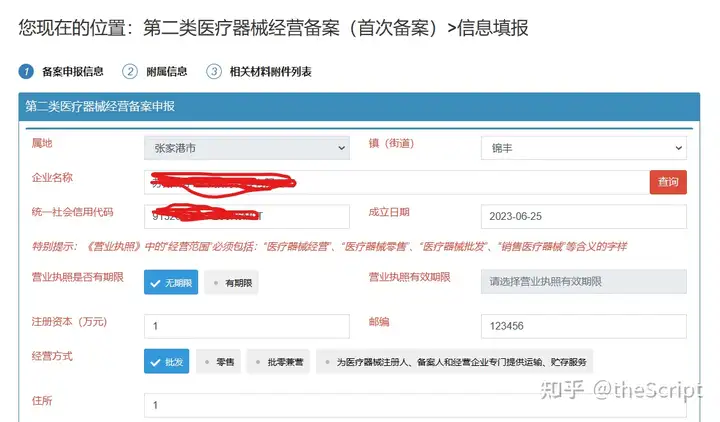
图7 信息填报
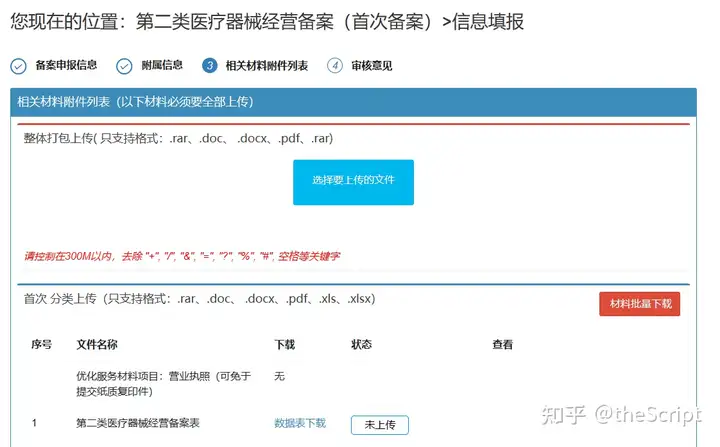
图8 上传附件
五、递交纸质材料和领取备案凭证
审批完成,系统状态显示受理中或者办件人员告知可以递交纸质材料后,递交纸质材料到窗口,便可以领取备案凭证了。
附件:法规依据(附链接)
关于实施《医疗器械经营质量管理规范》的通知 (适用于苏州)
第二类医疗器械经营备案材料须知(20220516版)(适用于苏州)
国家食品药品监督管理总局关于施行医疗器械经营质量管理规范的公告
医疗器械经营监督管理办法
医疗器械注册与备案管理办法
医疗器械生产监督管理办法
医疗器械监督管理条例
| 法定代表人 | 田经理 | ||
| 注册资本 | 50 | ||
| 主营产品 | 医疗器械经营许可证代办,劳务派遣经营许可证代办,人力资源许可证代办,海关备案代办,进出口权备案,验资报告及各类许可证代办,企业进出口经营权备案、企业财务咨询及代办、工商办理和公司注册等 | ||
| 经营范围 | 一般项目:企业管理;企业管理咨询;市场主体登记注册代理;财务咨询;税务服务;商务代 理代办服务;信息技术咨询服务。(除依法须经批准的项目外,凭营业执照依法自主开展经营活 动)许可项目:代理记账。(依法须经批准的项目,经相关部门批准后方可开展经营活动, | ||
| 公司简介 | 我们公司专注于商业服务,商务服务,许可类资质,建筑类资质办理,注册资金为人民币10万元,雇员数量为11--30人,年营业额为:人民币150万元,我们的主营业务有:各类许可证代办,公司出具验资报告,公司各类许可证,企业进出口经营权备案、企业财务咨询及代办、工商办理和公司注册等,我们是服务型公司,如果您有任何问题可以联系我。下面是我们公司的一些产品信息,您可以参考,同时更多信息也可以联系我的电话。公司 ... | ||
- 2025年快速办理进出口备案流程、条件及所需资料概览在全球贸易一体化的背景下,进出口备案已经成为每个希望开展国际业务的企业必须面对的... 2025-01-09
- ✨全国进出口经营权备案新办和变更!在全球经济不断发展的今天,进出口贸易成为了许多企业实现跨国经营的重要途径。为了推... 2025-01-09
- ✨终于有人把外贸进出口备案讲清楚了!--营业执照+进出口通办专办在当今全球化的市场环境中,越来越多的企业开始关注外贸进出口业务。对于许多企业来说... 2025-01-09
- 🚀陕西西安对外贸易经营者备案登记全攻略想要开展对外贸易业务?首先,你需要完成对外贸易经营者备案登记。下面是详细的步骤和... 2025-01-09
- 2025年在陕西进出口权备案操作流程✌一、进出口权备案的意义进出口权备案是国家为了加强对外贸易管制,规范进出口企业的经... 2025-01-09
 第二类医疗器械经营备案凭证变更受理条件有哪些?办理时间:3-5天
第二类医疗器械经营备案凭证变更受理条件有哪些?办理时间:3-5天 办理二类医疗器械经营备案凭证时,质量负责人一定要是医学专业的吗?办理时间:3-5天
办理二类医疗器械经营备案凭证时,质量负责人一定要是医学专业的吗?办理时间:3-5天 商洛-第二类医疗器械经营备案变更办理流程细节指南来了办理时间:3-5天
商洛-第二类医疗器械经营备案变更办理流程细节指南来了办理时间:3-5天 【第二类医疗器械经营备案】变更经营范围的流程办理时间:3-5天
【第二类医疗器械经营备案】变更经营范围的流程办理时间:3-5天 第二类医疗器械经营备案变更办事指南(简版)办理时间:3-5天
第二类医疗器械经营备案变更办事指南(简版)办理时间:3-5天 经营范围变更后原第二医疗器械经营备案凭证要重新办理吗?办理时间:3-5天
经营范围变更后原第二医疗器械经营备案凭证要重新办理吗?办理时间:3-5天 汉中_第二类医疗器械经营备案变更需要提交材料目录办理时间:3-5天
汉中_第二类医疗器械经营备案变更需要提交材料目录办理时间:3-5天 安康_医疗器械经营企业许可证(第二、三类)变更经营范围应该提交哪些材料?办理时间:3-5天
安康_医疗器械经营企业许可证(第二、三类)变更经营范围应该提交哪些材料?办理时间:3-5天 榆林_第二类医疗器械经营备案(变更)办理条件是什么?办理时间:3-5天
榆林_第二类医疗器械经营备案(变更)办理条件是什么?办理时间:3-5天 延安_三类医疗器械经营许可证如何变更--加急办理快速下证办理时间:3-5天
延安_三类医疗器械经营许可证如何变更--加急办理快速下证办理时间:3-5天





